自2017年,FDA批准上市了两款靶向CD19的CAR-T产品Yescarta和Kymriah,在肿瘤免疫治疗上取得一定成功,但这种细胞制备主要有下列几个问题亟待解决1)细胞制备主要依赖于患者自体T细胞,质量不一;2)自体CAR-T制备时间较长、流程复杂、价格昂贵;3)存在细胞因子释放综合征(CRS)、神经毒性、脱靶效应等副作用。因此,其安全性低,且无法做到“现货”供应。为了解决这些问题,同种异体移植细胞治疗的发展成为肿瘤免疫治疗的主要方向之一。
自然杀伤(natural killer,NK)细胞具有MHC非限制性,可通过各种NK受体(NKp46, NKp44,NKp30,NKG2D, DNAM-1)杀伤肿瘤细胞,并且可通过CD16具有抗体依赖的细胞介导的细胞毒性活性,将CAR安装到NK细胞上,在肿瘤免疫治疗中显示出较大的潜力(图1)[1]。
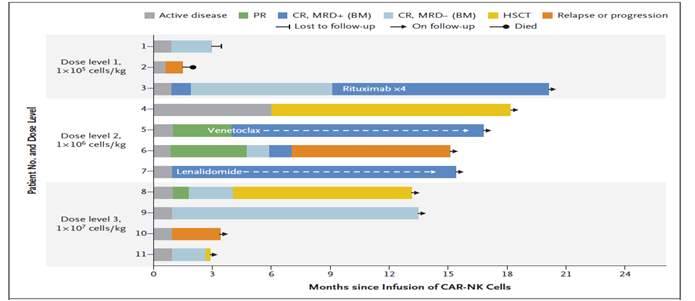
在2020年,德克萨斯大学M.D.安德森癌症中心公布美国首个CAR-NK细胞临床试验(NCT03056339)的结果。研究表明,脐带血(UCS)来源的CAR-NK细胞疗法治疗既往接受过治疗的复发性非霍奇金淋巴瘤(NHL)和慢性淋巴细胞白血病(CLL)患者,在13.9个月的随访期间,11名治疗患者中的8名(73%)有客观缓解(5名CLL患者中的4名,6名非霍奇金淋巴瘤患者中的4名),11名患者中的7名(64%)完全缓解。在安全性方面,在HLA完全不匹配的情况下,未发生移植物抗宿主病(GVHD),并且未观察到严重的CRS或神经毒性。主要的的原因与细胞本身不分泌过高的IL-6等细胞因子有关,未造成严重副作用(图2)。
图2:脐带血来源CAR-NK疗法的临床响应和缓解后治疗
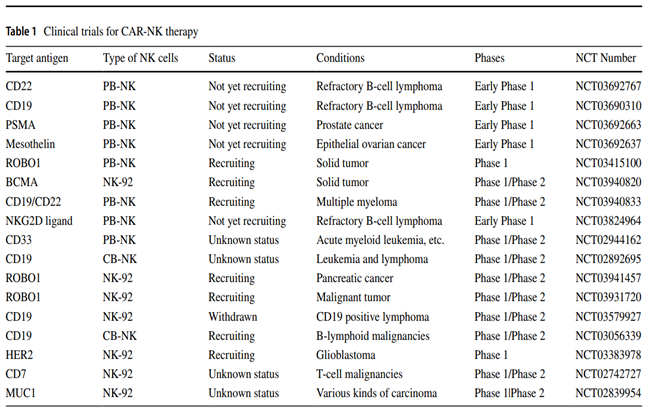
除了上述UCS来源的CAR-NK之外,还可以来源于健康供者周边血液(PB)、NK细胞系、NK-92、人类胚胎干细胞(hESCs)以及诱导多能干细胞(iPSC),部分已进入临床试验阶段(附表)。
干细胞具备自我更新能力,提供无限生长且质量稳定的细胞来源。其中,iPSCs来源的CAR-NK更易获得;可进行KIR单倍型检测;并逃避T细胞识别;可被克隆。2018年,在《StemCells》期刊上发表的一项研究中表明,经过CAR修饰的来源于iPSCs的NK细胞,在小鼠卵巢癌模型中表现出增强的抗肿瘤活性[2]。2019年,美国FDA已批准Fate Therapeutics 公司iPSCs来源的CAR-NK FT500、FT516、FT596三项研究性新药申请,已进入临床试验阶段。FT500可以与T细胞协同作用,激活抗PD-1或抗PDL-1疗法的实体瘤患者的免疫系统。并且,FT500可以冷冻保存,用于重复临床给药。FT596是一种含有三种活性抗肿瘤成分的细胞疗法,其独特的设计旨在克服CD19抗原逃逸,靶向多种抗原,最大限度地发挥治疗的效力和最小化毒性[3-4]。2019年,来自于日本的研究者们在Cell Stem Cell上发表一篇关于使用来自HLA-A24纯合子供体的iPCS所构建的iCAR-NK/ ILCs,并应用于GPC3阳性卵巢肿瘤(KOC7c)异种移植小鼠模型,研究表明可抑制肿瘤生长,延长小鼠生存时间。除疗效外,iCAR-NK/ ILCs在应用于免疫缺陷小鼠进行非临床安全性评估时,未表现出系统性、急性毒性或致瘤性[5],下一步将进入临床试验进行验证。
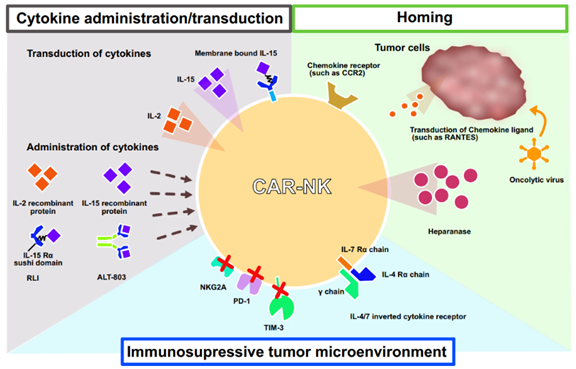
肿瘤的异质性是实体瘤治疗的主要困难点之一,无论是CAR-T或CAR-NK,单一靶点的CAR免疫细胞都不能完全清除所有的实体肿瘤细胞。因此,iPSCs来源的CAR-NK还需要进一步改造,主要从细胞因子转导、改善归巢能力、肿瘤微环境入手,来达到更好的肿瘤清除效果(图3)。
感想:CAR-NK细胞免疫疗法较目前市面上的自体CAR-T细胞治疗具有许多优势,主要包括:成本较低、患者无须等待制备时间、毒副作用较低等。以CAR-NK为模式的临床试验,取得了一定的治疗效果。可以考虑根据不同肿瘤类型,设计不同抗原靶点CAR-NK。若希望制备成“现货”,除了上述的三点改造建议外,还需要考虑冻存后的细胞是否能达到相同的疗效;根据临床医生对患者肿瘤进展情况,考虑是否联合其他抗肿瘤药物联合治疗。
修改:刘宝瑞(南京大学医学院附属鼓楼医院肿瘤中心主任医师,博导)
[1]. Ueda T, Kaneko S. Induced pluripotent stem cell-derived natural killer cells gene-modified to express chimeric antigen receptor-targeting solid tumors. International Journal of Hematology. 2020 Jul 23.
[2]. Hermanson DL, Bendzick L, Pribyl L, et al. Induced pluripotent stem cell-derived natural killer cells for treatment of ovarian cancer. Stem Cells. 2016;34(1):93-101.
[3].Li Y, Hermanson DL, Moriarity BS, et al. Human iPSC-derived natural killer cells engineered with chimeric antigen receptors enhance anti-tumor activity. Cell Stem Cell.2018;23(2):181.e5-192.e5.
[4]. Liu E, Liu E, Marin D, et al. Use of CAR-transduced natural killer cells in CD19- positive lymphoid tumors. The New England journal of medicine. 2020; 382(6):545-553.
[5].Xu H, Wang B, Ono M, et al. Targeted Disruption of HLA Genes via CRISPR-Cas9 Generates iPSCs with Enhanced Immune Compatibility. Cell Stem Cell. 2019 Apr 4; 24(4):566-578.
南京大学鼓楼医院肿瘤中心 主任医师 教授
专注于肿瘤个体化及靶向药物治疗
新抗原疫苗及靶向免疫治疗
精准放疗及中西医结合治疗
原文始发于微信公众号(刘宝瑞肿瘤医疗网络平台):2020文献快递:CAR-NK“现货”细胞免疫疗法在肿瘤治疗方面优势显著







评论